ИНСТРУКЦИЯ по применению лекарственного препарата для медицинского применения Хумира®
Регистрационный номер
ЛС-002422-290915
Торговое наименование препарата
Хумира®
Международное непатентованное наименование или группировочное наименование
Адалимумаб
Лекарственная форма
Раствор для подкожного введения
Состав
В 0,8 мл раствора содержится:
Активное вещество: адалимумаб — 40,0 мг.
Вспомогательные вещества: маннитол — 9,6 мг; лимонной кислоты моногидрат — 1,044 мг; натрия цитрат — 0,244 мг; натрия гидрофосфата дигидрат — 1,224 мг; натрия дигидрофосфата дигидрат — 0,688 мг; натрия хлорид — 4,932 мг; полисорбат 80 — 0,8 мг; вода для инъекций — 759,028-759,048 мг; натрия гидроксид для коррекции рН — 0,02-0,04 мг.
Описание
Опалесцирующий слегка окрашенный раствор.
Фармакотерапевтическая группа
Иммунодепрессивное средство
Код АТХ
L04АВ04
Фармакологические свойства
Адалимумаб представляет собой рекомбинантное моноклинальное антитело, пептидная последовательность которого идентична IgG1 человека. Адалимумаб селективно связывается с фактором некроза опухоли альфа (ФНО-α) и нейтрализует его биологические функции за счет блокады взаимодействия с поверхностными клеточными р55 и р75 рецепторами к ФНО-α. ФНО-α — это естественный цитокин, который принимает участие в регуляции нормального воспалительного процесса и иммунного ответа. Повышенную концентрацию ФНО-α обнаруживают в синовиальной жидкости у пациентов с ревматоидным артритом, ювенильным идиопатическим артритом, псориатическим артритом и анкилозирующим спондилитом. ФНО-α играет важную роль в развитии патологического воспалительного процесса и разрушения суставной ткани, характерных для этих заболеваний. Повышенные концентрации ФНО-α также обнаруживаются в псориатических бляшках. При бляшечном псориазе лечение адалимумабом может привести к уменьшению толщины бляшек и инфильтрации воспалительными клетками. Взаимосвязь между данным клиническим эффектом адалимумаба и механизмом его действия не установлена.
Также адалимумаб модулирует биологические ответные реакции, которые усиливаются или регулируются ФНО-α, включая изменения уровней молекул адгезии, вызывающих миграцию лейкоцитов.
Фармакодинамика
У пациентов с ревматоидным артритом адалимумаб вызывал быстрое снижение концентрации острофазных показателей воспаления (С-реактивного белка (СРБ) и скорости оседания эритроцитов) и сывороточной концентрации цитокинов (интерлейкин-6). Уменьшение концентраций СРБ также наблюдалось у пациентов с ювенильным идиопатическим артритом, болезнью Крона, язвенным колитом. Кроме того, отмечалось снижение сывороточной активности матриксных металлопротеиназ (ММП-1 и ММП-3), вызывающих ремоделирование тканей, которое лежит в основе разрушения хрящевой ткани.
Фармакокинетика
Всасывание
Адалимумаб всасывается и распределяется медленно и достигает своей максимальной сывороточной концентрации примерно через 5 дней. Абсолютная биодоступность адалимумаба при однократном подкожном введении 40 мг составляет 64 %.
Распределение и выведение
Объем распределения (Vd) при однократном внутривенном введении составляет от 4,7 л до 6,0 л, что указывает на практически одинаковое распределение адалимумаба в крови и внесосудистых жидкостях. Адалимумаб выводится медленно, клиренс (Cl) обычно не превышает 12 мл/ч. Период полувыведения (T1/2) составляет, в среднем, 2 недели и варьирует от 10 до 20 дней. Cl и Т1/2 существенно не меняются при введении доз 0,25-10 мг/кг, а T1/2 сходен при внутривенном и подкожном введении адалимумаба. Концентрация адалимумаба в синовиальной жидкости у пациентов с ревматоидным артритом составляет 31% — 96% от таковой, в сыворотке.
Фармакокинетика адалимумаба в равновесном состоянии
Равновесные концентрации адалимумаба при подкожном введении в дозе 40 мг один раз в две недели у больных ревматоидным артритом в конце интервала дозирования составляли около 5 мкг/мл (без одновременного приема метотрексата (МТХ)) и 8-9 мкг/мл (на фоне одновременного применения МТХ). При увеличении дозы адалимумаба в интервале 20 мг, 40 мг и 80 мг один раз в две недели и один раз в неделю подкожно отмечено близкое к пропорциональному увеличение сывороточных концентраций адалимумаба в конце интервала дозирования. При длительном применении (более 2 лет) клиренс адалимумаба не изменялся.
При монотерапии адалимумабом (без метотрексата) в дозе 40 мг один раз в 2 недели средняя равновесная минимальная концентрация (Сmin) препарата у пациентов с псориазом составила 5 мкг/мл.
Отмечена тенденция к возрастанию Cl адалимумаба при увеличении массы тела и наличии антител к адалимумабу.
Для пациентов с болезнью Крона, со стартовой дозой 160 мг адалимумаба на 0-й неделе и с последующей дозой в 80 мг на 2-й неделе, адалимумаб достигает своей максимальной сывороточной концентрации (Сmax) (примерно 12 мкг/мл) на 2-й и 4-й неделе.
У пациентов с болезнью Крона равновесная концентрация (приблизительно 7 мкг/мл) наблюдается на 24-й и 56-й неделях поддерживающей терапии с применением 40 мг адалимумаба один раз в 2 недели.
У пациентов с язвенным колитом, получающих 160 мг адалимумаба исходно и 80 мг через 2 недели концентрация препарата в плазме крови составляла приблизительно 12 мкг/мл в течение индукционного периода. Равновесная концентрация составляла приблизительно 8 мкг/мл у пациентов, получавших поддерживающую дозу 40 мг 1 раз в 2 недели.
Дети
После введения 24 мг/м2 адалимумаба (максимум до 40 мг) подкожно один раз в две недели пациентам от 4 лет до 17 лет с ювенильным идиопатическим артритом средняя равновесная концентрация адалимумаба (измеренная с 20-й недели по 48-ю) в сыворотке крови составила 5,6 ± 5,6 мкг/мл (102% коэффициент вариации (CV)) при терапии препаратом Хумира® без метотрексата и 10,9 ± 5,2 мкг/мл (47,7% CV) с сопутствующей терапией метотрексатом. Средняя равновесная концентрация адалимумаба в сыворотке крови у пациентов с массой тела менее 30 кг, после введения препарата Хумира® в дозе 20 мг подкожно один раз в две недели, составляла 6,8 мкг/мл при терапии препаратом Хумира® без метотрексата и 10,9 мкг/мл при применении в комбинации с метотрексатом. Средняя равновесная концентрация адалимумаба в сыворотке крови у пациентов с массой тела 30 кг и более после введения препарата Хумира® в дозе 40 мг подкожно один раз в две недели составляла 6,6 мкг/мл при терапии препаратом Хумира® без метотрексата и 8,1 мкг/мл при применении в комбинации с метотрексатом. У пациентов в возрасте от 2 лет до 4 лет или от 4 лет и старше с массой тела менее 15 кг с ювенильным идиопатическим артритом средняя равновесная концентрация составляла 6,0 ± 6,1 мкг/мл (101 % CV) при терапии препаратом Хумира® без метотрексата и 7,9 ± 5,6 мкг/мл (71,2 % CV) при применении в комбинации с метотрексатом.
У пациентов детского возраста с болезнью Крона (среднетяжелой или тяжелой степени) после введения стартовой дозы адалимумаба 160/80 мг или 80/40 мг (в зависимости от массы тела) на 0-й неделе и 2-й неделе, и далее с применением поддерживающих доз 40/20 мг или 20/10 мг один раз в 2 недели (в зависимости от массы тела), средняя концентрация адалимумаба в сыворотке крови (с учетом стандартного отклонения) на 4-ой неделе применения составляла 15,7 ± 6,6 мкг/мл (у пациентов с массой тела от 40 кг и более) и 10,6 ± 6,1 мкг/мл (у пациентов с массой тела менее 40 кг).
Особые группы пациентов
Пожилые пациенты
Возраст оказывает минимальное влияние на Cl адалимумаба.
Пол, раса
Различий в показателях фармакокинетики (с поправкой на массу тела) у пациентов разного пола и расовой принадлежности не выявлено.
Печеночная и почечная недостаточность
Сведений о фармакокинетике адалимумаба у больных с нарушением функции печени или почек нет.
Показания к применению
Взрослые
• Среднетяжелый и тяжелый активный ревматоидный артрит (в режиме монотерапии или в комбинации с метотрексатом или другими базисными противовоспалительными препаратами).
• Активный псориатический артрит (в режиме монотерапии или в комбинации с метотрексатом или другими базисными противовоспалительными препаратами).
• Активный анкилозирующий спондилит.
• Болезнь Крона (среднетяжелой или тяжелой степени):
— при неадекватном ответе на традиционную терапию, а также непереносимости или противопоказаниях к традиционной терапии;
— при неэффективности (или снижении эффективности) или непереносимости инфликсимаба.
• Хронический бляшечный псориаз (среднетяжелой и тяжелой степени), когда показана системная терапия или фототерапия и когда другие варианты системной терапии не являются оптимальными.
• Язвенный колит среднетяжелой и тяжелой степени, при неадекватном ответе на традиционную терапию, включая кортикостероиды и/или 6-меркаптопурин или азатиоприн, а также при непереносимости или противопоказаниях к традиционной терапии.
Дети
• Ювенильный идиопатический артрит у пациентов от 2 лет в режиме монотерапии или в комбинации с метотрексатом.
• Болезнь Крона (среднетяжелой или тяжелой степени) у пациентов от 6 лет и старше при неадекватном ответе на традиционную терапию, а также непереносимости или противопоказаниях к традиционной терапии.
Противопоказания
• Гиперчувствительность к адалимумабу или любым его вспомогательным компонентам.
• Беременность.
• Период грудного вскармливания.
• Детский возраст до 18 лет, кроме пациентов от 2 лет с ювенильным идиопатическим артритом и пациентов от 6 лет и старше с болезнью Крона (среднетяжелой или тяжелой степени).
• Инфекционные заболевания, в том числе туберкулез.
• Совместный прием с антагонистами ФНО или другими генно-инженерными биологическими противоревматическими препаратами (например, анакинра и абатацепт).
С осторожностью
• Рецидивирующие инфекции в анамнезе.
• Носительство вируса гепатита В.
• Злокачественные новообразования, в том числе в анамнезе.
• Сердечная недостаточность.
• Демиелинизирующие заболевания нервной системы, в том числе в анамнезе.
• Пациенты старше 65 лет.
Применение при беременности и в период грудного вскармливания
В исследованиях на животных в дозах до 100 мг/кг признаков негативного действия адалимумаба на плод выявлено не было. Однако в доказательных контролируемых исследованиях у беременных женщин препарат не изучался, поэтому применение адалимумаба противопоказано при беременности. Женщинам репродуктивного возраста следует избегать беременности во время лечения адалимумабом.
Сведений о выведении адалимумаба с грудным молоком или его всасывании после приема внутрь нет.
Многие человеческие иммуноглобулины проникают в грудное молоко. Учитывая риск развития серьезных побочных реакций у новорожденного, кормление грудью не рекомендуется в период лечения адалимумабом и в течение как минимум пяти месяцев после последней инъекции адалимумаба. Решение о прекращении кормления или о прекращении лечения адалимумабом необходимо принимать, основываясь на важности продолжения терапии для матери.
Роды
Влияние адалимумаба на родовую деятельность и роды неизвестно.
Способ применения и дозы
Подкожно.
Лечение препаратом Хумира® проводится под контролем врача. Если врач считает это возможным, то после соответствующего обучения технике подкожных инъекций, больные могут самостоятельно вводить себе препарат.
Препарат Хумира® вводят подкожно в область бедра или живота. Раствор следует осмотреть перед введением на предмет наличия посторонних частиц и изменения цвета.
Адалимумаб не следует смешивать в одном шприце или флаконе с любыми другими лекарственными препаратами. Оставшийся раствор и использованные материалы следует утилизировать.
Если очередная инъекция препарата Хумира® была случайно пропущена, необходимо провести инъекцию сразу, как только это будет обнаружено. Следующая инъекция должна быть проведена в соответствии с запланированным ранее графиком.
Взрослые
Ревматоидный артрит (PA), псориатический артрит (ПсА) и анкилозирующий спондилит (АС)
Рекомендуемая доза препарата Хумира® у взрослых с ревматоидным артритом (РА), псориатическим артритом (ПсА) и анкилозирующим спондилитом (АС) составляет 40 мг подкожно один раз в две недели. При назначении препарата Хумира® терапия глюкокортикостероидами, нестероидными противовоспалительными препаратами (в т.ч. салицилатами), анальгетиками (наркотическими и ненаркотическими), метотрексатом и другими базисными противоревматическими препаратами может быть продолжена.
У некоторых больных с ревматоидным артритом, не получающих метотрексат, дополнительный эффект может быть достигнут при увеличении кратности применения препарата Хумира® до 40 мг один раз в неделю.
Болезнь Крона
Рекомендуемый режим дозирования препарата Хумира® для взрослых с болезнью Крона — 160 мг в 1-й день (применяется по четыре инъекции по 40 мг в день или по две инъекции по 40 мг в день последовательно в течение двух дней), через 2 недели (на 15-й день) — 80 мг, еще через 2 недели (29-й день) начинают применять поддерживающую дозу — 40 мг один раз в 2 недели. При назначении препарата Хумира® терапия аминосалицилатами, глюкокортикостероидами, и/или иммуномодуляторами (например: 6-меркаптопурин и азатиоприн) может быть продолжена.
Пациенты, наблюдающие уменьшение ответа на лечение препаратом, могут получить дополнительный эффект от увеличения частоты введения препарата Хумира® до 40 мг одного раз в неделю.
Некоторые пациенты могут не отвечать на терапию препаратом Хумира® в течение первых четырех недель, однако лечение следует продолжить, т.к. положительный эффект может быть достигнут в течение 12 недель. Решение о прекращении терапии может быть принято в случае, если пациент не получает эффекта от лечения в течение этого периода.
Язвенный колит
Начальная (индукционная) доза для взрослых со среднетяжелой и тяжелой степенью язвенного колита составляет 160 мг исходно (доза может быть введена в виде четырех инъекций в один день в виде двух инъекций в сутки в течение двух дней подряд) и 80 мг через 2 недели. После индукционной дозы рекомендуемая поддерживающая доза составляет 40 мг, которая вводится в виде регулярных подкожных инъекций с интервалом в 2 недели. Во время лечения препаратом Хумира® терапия аминосалицилатами, кортикостероидами и/или иммуномодуляторами (например, 6-меркаптопурином и азатиоприном) может быть продолжена.
На фоне поддерживающего лечения препаратом Хумира® доза кортикостероидов может снижаться вплоть до полной отмены в соответствии с имеющимися клиническими руководствами по лечению язвенного колита.
Пациенты, у которых наблюдается уменьшение ответа на лечение препаратом, могут получить дополнительный эффект от увеличения частоты введения препарата Хумира® до одного раза в неделю.
Имеющиеся данные свидетельствуют о том, что клинический эффект обычно достигается в течение 2-8 недель лечения. Лечение препаратом Хумира® следует продолжать только у пациентов, у которых наблюдается терапевтический эффект в течение первых 8 недель терапии.
Хронический бляшечный псориаз
Начальная доза для взрослых пациентов составляет 80 мг.
Поддерживающая доза — по 40 мг раз в две недели, начиная через неделю после начальной дозы.
Дети
Ювенильный идиопатический артрит
Применение препарата Хумира® у детей младше 2 лет с ювенильным идиопатическим артритом не изучалось.
При ювенильном идиопатическом артрите у детей в возрасте от 2 лет до 12 лет препарат Хумира® назначают в дозе 24 мг/м2 площади поверхности тела, при этом максимальная однократная доза составляет
для детей от 2 до 4 лет — 20 мг;
для детей от 4 до 12 лет — 40 мг.
Препарат вводят подкожно 1 раз в 2 недели. Объем инъекции определяют исходя из роста и веса пациента (см. Таблицу 1).
Для пациентов, которым необходимо введение менее 40 мг препарата, необходимо использовать препарат Хумира® во флаконе.
Таблица 1.
Дозы препарата Хумира® в миллилитрах (мл) исходя из роста и веса пациентов детского возраста, страдающих ювенильным идиопатическим артритом
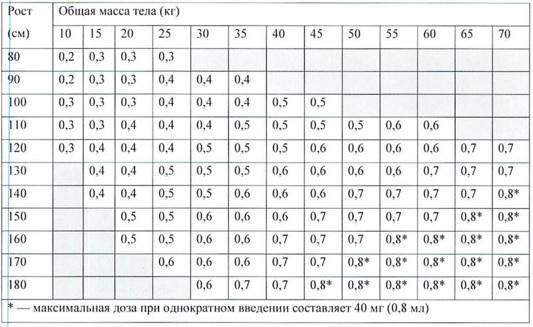
Подросткам от 13 лет назначают по 40 мг раз в 2 недели вне зависимости от площади поверхности тела.
Клинический ответ обычно достигается в течение 12 недель лечения. Решение о прекращении терапии может быть принято в случае, если пациент не получает эффекта от лечения в течение этого периода.
Болезнь Крона
Пациенты с массой тела менее 40 кг: 80 мг в 1-й день (применяется по две инъекции по 40 мг в день), через 2 недели (на 15-й день) — 40 мг, еще через 2 недели (29-й день) начинают применять поддерживающую дозу по следующей схеме — 20 мг один раз в 2 недели (среднетяжелая и тяжелая степень).
Пациенты с массой тела 40 кг и более: 160 мг в 1-й день (применяется по четыре инъекции по 40 мг в день или по две инъекции по 40 мг в день последовательно в течение двух дней), через 2 недели (на 15-й день) — 80 мг, еще через 2 недели (29-й день) начинают применять поддерживающую дозу по следующей схеме:
болезнь Крона тяжелой степени — 40 мг один раз в 2 недели;
болезнь Крона среднетяжелой степени —20 мг один раз в 2 недели.
Пациенты, у которых наблюдается уменьшение ответа на лечение препаратом, могут получить дополнительный эффект от увеличения частоты введения препарата Хумира® до одного раза в неделю.
Клинический ответ обычно достигается в течение 12 недель лечения. Решение о прекращении терапии может быть принято в случае, если пациент не получает эффекта от лечения в течение этого периода.
Применение препарата Хумира® у детей младше 6 лет с болезнью Крона не изучалось.
Инструкцию по подготовке и проведению инъекции препарата Хумира® смотрите в информационном листке, вложенном в картонную пачку.
Побочное действие
Данные клинических исследований
Приблизительно у 13% пациентов можно ожидать развития реакций в месте введения препарата (одни из наиболее часто встречающихся побочных реакций при введении адалимумаба в контролируемых клинических исследованиях).
Побочные реакции возможно причинно-связанные с применением препарата, как клинические, так и лабораторные, приведены ниже с указанием частоты (очень часто ≥ 1/10, часто ≥ 1/100, но < 1/10, нечасто ≥ 1/1000, но < 1/100, редко ≥ 1/10000, но < 1/1000).
Включалась наивысшая частота, наблюдаемая среди различных показаний.
Инфекции
Очень часто: инфекции дыхательных путей (включая инфекции верхних и нижних дыхательных путей, пневмонию, синусит, фарингит, назофарингит и герпес-вирусную пневмонию).
Часто: генерализованные инфекции (включая сепсис, кандидоз и грипп), инфекции ЖКТ (включая вирусный гастроэнтерит), инфекции кожи и мягких тканей (включая паронихий, целлюлит, импетиго, некротизирующий фасциит и опоясывающий лишай), инфекции уха, инфекции полости рта (включая простой герпес, оральный герпес и поражения зубов), инфекции половой сферы (включая вульвовагинальную микотическую инфекцию), инфекции мочевыделительного тракта (включая пиелонефрит), грибковые инфекции, инфекции суставов.
Нечасто: оппортунистические инфекции и туберкулез (включая кокцидиомикоз, гистоплазмоз и комплекс инфекций, вызываемых Mycobacterium avium), неврологические инфекции (включая вирусный менингит), инфекции глаза, бактериальные инфекции.
Новообразования
Часто: доброкачественные новообразования, рак кожи, кроме меланомы (включая базально-клеточную карциному и чешуйчато-клеточную карциному).
Нечасто: лимфома, паренхиматозные новообразования (включая рак молочной железы, новообразования легкого и щитовидной железы), меланома.
Со стороны крови и лимфатической системы
Очень часто: лейкопения (включая нейтропению и агранулоцитоз), анемия.
Часто: тромбоцитопения, лейкоцитоз.
Нечасто: идиопатическая тромбоцитопеническая пурпура.
Редко: панцитопения.
Со стороны иммунной системы
Часто: реакции гиперчувствительности, аллергические реакции (включая сезонную аллергию).
Со стороны обмена веществ
Очень часто: повышение концентрации липидов.
Часто: гипокалиемия, повышение концентрации мочевой кислоты, аномальные концентрации натрия, гипокальциемия, гипергликемия, гипофосфатемия, дегидратация.
Нарушения психики
Часто: изменения настроения (включая депрессию), тревожные расстройства, бессонница.
Со стороны нервной системы
Очень часто: головная боль.
Часто: парестезии (включая гипестезии), мигрень, невралгия седалищного нерва, вестибулярное головокружение.
Нечасто: тремор, нейропатия.
Редко: рассеянный склероз.
Со стороны органов чувств
Часто: конъюнктивит, нарушения зрения, блефарит, отек века.
Нечасто: диплопия, глухота, звон в ушах.
Со стороны сердечно-сосудистой системы
Часто: повышение артериального давления, приливы, гематомы, тахикардия.
Нечасто: аритмия, застойная сердечная недостаточность, артериальная окклюзия, тромбофлебит, аневризма аорты.
Редко: остановка сердца.
Со стороны системы дыхания
Часто: кашель, астма, диспноэ.
Нечасто: хроническая обструктивная болезнь легких, интерстициальные заболевания легких, пневмонит.
Со стороны системы пищеварения
Очень часто: тошнота, рвота, боль в животе, повышение активности печеночных ферментов.
Часто: диспепсия, гастроэзофагеальный рефлюкс, сухость во рту, желудочно-кишечные кровотечения.
Нечасто: панкреатит, дисфагия, отек лица, холецистит, холелитиаз, повышение концентрации билирубина, печеночный стеатоз.
Со стороны кожи и подкожных тканей
Очень часто: сыпь (в т.ч. эксфолиативная).
Часто: зуд, крапивница, кровоизлияния (в т.ч. пурпура), дерматит (в т.ч. экзема), ломкость ногтей, гипергидроз.
Нечасто: ночная потливость, рубцы.
Со стороны костно-мышечной системы
Очень часто: костно-мышечная боль.
Часто: мышечные спазмы.
Нечасто: рабдомиолиз, системная красная волчанка.
Со стороны мочеполовой системы
Часто: гематурия, почечная недостаточность.
Нечасто: никтурия, эректильная дисфункция.
Прочие, включая реакции в месте введения
Очень часто: реакции в месте инъекции (включая эритему).
Часто: боль в грудной клетке, отеки, ухудшение заживления ран.
Нечасто: воспаление.
Лабораторные показатели
Часто: нарушения в системе свертывания крови (включая увеличение активированного частичного тромбопластинового времени), положительные тесты на аутоантитела (включая антитела к двойной спирали ДНК), увеличение концентрации лактатдегидрогеназы.
Клинические испытания у детей
В основном, побочные реакции у детей были одинаковыми по типу и частоте с теми, которые наблюдались у взрослых.
Реакции в месте инъекции
В базовых исследованиях у 12,9% пациентов, которым вводили адалимумаб, развились реакции в месте введения (эритема и/или зуд, кровотечение, боль, припухлость), в контрольной группе такие реакции развились у 7,1% пациентов. Большинство реакций в месте инъекций оценивались как слабые и не требовали прекращения приема препарата.
Инфекции
В контролируемых исследованиях уровень инфекционных осложнений составлял 1,51 на одного пациента в год при лечении адалимумабом и 1,46 на одного пациента в год в контрольной группе пациентов (взрослого и детского возрастов). Частота серьезных инфекционных осложнений составляла 0,04 на одного пациента в год при лечении адалимумабом и 0,03 на одного пациента в год в контрольной группе пациентов. Инфекционные осложнения были в большинстве случаев представлены инфекциями верхних дыхательных путей, назофарингитом, синуситом, бронхитом и инфекциями мочевыделительного тракта. Большинство пациентов продолжали принимать адалимумаб после разрешения инфекции.
В контролируемых открытых исследованиях применения адалимумаба сообщалось о серьезных инфекциях (включая редко возникающие смертельные инфекции), в частности о туберкулезе (включая милиарный и внелегочный), легионеллезе и инвазивных оппортунистических инфекциях (в том числе диссеминированном гистоплазмозе, пневмоцистной пневмонии, аспергиллезе и листериозе).
Злокачественные новообразования и лимфопролиферативные расстройства
В клинических исследованиях у 249 пациентов с ЮИА не наблюдалось злокачественных новообразований при наблюдении в течение 655,6 пациенто-лет.
В клинических исследованиях у 192 пациентов детского возраста с болезнью Крона не наблюдалось злокачественных новообразований при наблюдении в течение 258,9 пациенто-лет.
Во время контролируемых этапов базовых испытаний применения адалимумаба продолжительностью по меньшей мере 12 недель у пациентов с РА, ПсА, АС, болезнью Крона, язвенным колитом и псориазом с активностью от слабой до сильно выраженной злокачественные новообразования, за исключением лимфомы и немеланомного рака кожи, наблюдались с частотой (95% доверительный интервал) 6,1 (3,8-9,9) на 1000 пациенто-лет среди 5041 пациентов, принимавших адалимумаб по сравнению с 6,9 (3,7-12,7) на 1000 пациенто-лет среди 3194 пациентов контрольной группы (средняя продолжительность лечения составляла 4,0 месяцев при применении адалимумаба и 3,9 месяца в контрольной группе пациентов).
Частота (95 % доверительный интервал) рака кожи, кроме меланомы, составляла 9,0 (6,1-13,3) на 1000 пациенто-лет среди пациентов, принимавших адалимумаб, и 3,4 (1,4-8,2) на 1000 пациенто-лет среди пациентов контрольной группы. Из общего числа случаев рака кожи чешуйчато-клеточные карциномы возникали с частотой (95 % доверительный интервал) 2,5 (1,2-5,3) на 1000 пациенто-лет среди пациентов, принимавших препарат адалимумаб, и 0,7 (0,1-4,9) на 1000 пациенто-лет среди пациентов контрольной группы.
Частота (95 % доверительный интервал) лимфом составляла 0,7 (0,2-2,9) на 1000 пациенто-лет среди пациентов, применявших адалимумаб, и 0,7 (0,1-4,9) на 1000 пациенто-лет среди пациентов в контрольной группе.
Наблюдаемая частота злокачественных новообразований, за исключением лимфом и немеланомного рака кожи, составляла около 8,5 на 1000 пациенто-лет в контролируемых фазах клинических испытаний, а также в продолжающихся и завершенных открытых исследованиях. Наблюдаемая частота рака кожи (кроме меланомы) составляла около 9,7 на 1000 пациенто-лет, наблюдаемая частота лимфомы — около 1,3 на 1000 пациенто-лет. Средняя продолжительность этих исследований составляла около 3,4 лет и включала 6008 пациентов, которые принимали адалимумаб по меньшей мере 1 год или у которых развилось злокачественное новообразование в течение 1 года от начала терапии, охватывая 25446 пациенто-лет.
Аутоантитела
На I-V этапах исследования РА проводился анализ сыворотки крови пациентов на аутоантитела. В достоверных контролируемых испытаниях сообщалось, что у 11,9 % пациентов, которые принимали препарат адалимумаб, и у 8,1% пациентов, принимавших плацебо, и пациентов контрольной группы, у которых были изначально отрицательные титры антинуклеарных антител, положительные титры появились на 24 неделе. У двоих из 3989 пациентов, принимавших адалимумаб в исследованиях РА, ПсА и АС, развились клинические проявления волчаночно-подобного синдрома. Состояние пациентов улучшилось после отмены лечения. Ни у одного из пациентов не развился люпус-нефрит или симптомы поражения центральной нервной системы. Влияние длительного применения адалимумаба на развитие аутоиммунных заболеваний остается неизученным.
Псориаз: развитие или ухудшение
Описываются случаи появления псориаза, включая пустулезный псориаз и ладонно-подошвенный псориаз, и случаи ухудшения существующего псориаза при применении всех блокаторов ФНО, включая адалимумаб. Многие из этих пациентов принимали иммунодепрессанты (в том числе, МТХ, кортикостероиды) в качестве сопутствующего лечения. Некоторым из этих пациентов требовалась госпитализация. У большинства пациентов наступило улучшение состояния после отмены блокаторов ФНО. У некоторых пациентов наступил рецидив псориаза после повторного начала приема различных блокаторов ФНО. Отмена адалимумаба должна осуществляться в тяжелых случаях и тогда, когда нет улучшения, либо есть ухудшение в ответ на проводимое местное лечение.
Ниже перечислены побочные реакции, указанные по системам органов, частота и связь которых с приемом препарата не доказана.
Повышение активности ферментов печени
В контролируемых исследованиях III фазы препарата Хумира® (40 мг подкожно 1 раз в две недели) у пациентов с РА и ПсА с длительностью контрольного периода от 4 до 104 недель, повышение активности АЛТ ≥ 3 верхней границы нормы (ВГН) было зарегистрировано у 3,7% пациентов, получавших препарат Хумира® и у 1,6% пациентов контрольной группы. В связи с тем, что многие пациенты в этих исследованиях также принимали лекарственные препараты, которые вызывают повышение активности ферментов печени (например, НПВС, метотрексат), взаимосвязь между препаратом Хумира® и повышением активности ферментов печени не ясна. В контролируемых исследованиях III фазы препарата Хумира® (первоначальная доза 160 мг и 80 мг, или 80 мг и 40 мг в дни 1 и 15, соответственно, а затем 40 мг каждые две недели) у пациентов с болезнью Крона с длительностью контрольного периода от 4 до 52 недель, повышение АЛТ ≥ 3 × ВГН было зарегистрировано у 0,9% пациентов, получавших препарат Хумира®, и у 0,9% пациентов контрольной группы. В контролируемых исследованиях III фазы препарата Хумира® (первоначальная доза 160 мг и 80 мг в дни 1 и 15 соответственно, а затем 40 мг каждые две недели) у пациентов с язвенным колитом с длительностью контрольного периода от 1 до 52 недель повышение активности АТ ≥3 ВГН было зарегистрировано у 1,5% пациентов, получавших препарат Хумира®, и у 1,0% пациентов контрольной группы. В контролируемых исследованиях III фазы препарата Хумира® (первоначальная доза 80 мг, затем 40 мг каждые две недели) у пациентов с бляшечным псориазом с длительностью контрольного периода от 12 до 24 недель, повышение активности AJIT ≥ 3 × ВГН было зарегистрировано у 1,8% пациентов, получавших препарат Хумира®, и у 1,8% пациентов контрольной группы.
В контролируемых исследованиях III фазы препарата Хумира® (40 мг 1 раз в две недели) у пациентов с аксиальным спондилоартритом (анкилозирующий спондилит и нерентгенологический аксиальный спондилоартрит) с длительностью контрольного периода от 12 до 24 недель, повышение активности АЛТ ≥ 3 × ВГН было зарегистрировано у 2,1% пациентов, получавших препарат Хумира®, и у 0,8% пациентов контрольной группы.
В контролируемых исследованиях III фазы препарата Хумира® у пациентов с ювенильным идиопатическим артритом в возрасте от 4 до 17 лет и у пациентов с энтезитассоциированным артритом в возрасте от 6 до 17 лет повышение активности АЛТ ≥ 3 × ВГН было зарегистрировано у 6,1% пациентов, получавших препарат Хумира®, и у 1,3% пациентов контрольной группы. Большинство случаев повышения активности АЛТ были зарегистрированы при одновременно использовании метотрексата. В исследовании III фазы препарата Хумира® у пациентов с полиартикулярным ювенильным идиопатическим артритом в возрасте от 2 до 4 лет случаев повышения активности АЛТ не зарегистрировано.
В исследовании III фазы препарата Хумира® у детей с болезнью Крона, в котором оценивались эффективность и безопасность двух поддерживающих дозовых схем (скорректированных на основании массы тола) после индукционной терапии, общая продолжительность периода лечения в котором составляла до 52 недель, повышение активности АЛТ ≥ 3 × ВГН было зарегистрировано у 2,6% (5/192) пациентов, из которых 4 пациентов на момент начала исследования получали сопутствующее лечение иммуносупрессорами.
При всех показаниях в клинических исследованиях повышение активности АЛТ у пациентов не сопровождалось симптомами, и в большинстве случаев носило преходящий характер и разрешалось без прекращения лечения. Тем не менее, в постмаркетинговом периоде были получены очень редкие сообщения о тяжелых печеночных реакциях, включая печеночную недостаточность у пациентов, получающих антагонисты ФНО, в том числе адалимумаб. Причинно-следственная связь таких реакций с лечением адалимумабом остается неясной.
Данные постмаркетинговых исследований
Инфекции и инвазии
Дивертикулит.
Новообразования доброкачественные, злокачественные и неклассифицированные (включая кисты и полипы)
Гепатоспленарная Т-клеточная лимфома, лейкемия, карцинома Меркеля (нейроэндокринная кожная карцинома).
Со стороны иммунной системы
Анафилаксия, саркоидоз.
Со стороны нервной системы
Демиелинизирующие заболевания (в том числе неврит зрительного нерва, синдром Гиена-Барре), цереброваскулярные расстройства.
Со стороны сердечно-сосудистой системы
Легочная эмболия, инфаркт миокарда.
Со стороны системы дыхания
Плевральный выпот, легочный фиброз.
Со стороны системы пищеварения
Перфорация кишечника, реактивация вируса гепатита В, печеночная недостаточность, гепатит.
Со стороны кожи и подкожных тканей
Кожный васкулит, синдром Стивенса Джонсона, отек Квинке (ангионевротический отек), возникновение или ухудшение псориаза (включая ладонно-подошвенный пустулярный псориаз), мультиформная эритема, алопеция.
Со стороны костно-мышечной системы и соединительной ткани
Волчаночноподобный синдром.
Прочие, включая реакции в месте введения
Повышение температуры тела.
Передозировка
Максимальная переносимая доза адалимумаба у человека не установлена. Повторное применение адалимумаба в дозах до 10 мг/кг не сопровождалось токсическими эффектами, требовавшими уменьшения дозы. В случае передозировки необходимо контролировать побочные реакции и немедленно начинать адекватное симптоматическое лечение.
Взаимодействие с другими лекарственными средствами
У больных ревматоидным артритом, получающих метотрексат нет необходимости в коррекции дозы адалимумаба или метотрексата. Вместе с тем метотрексат при однократном и повторном применении снижает клиренс адалимумаба на 29% и 44% соответственно.
Взаимодействие адалимумаба с другими препаратами, помимо метотрексата, в фармакокинетических исследованиях не изучалось. В клинических исследованиях не отмечено признаков взаимодействия адалимумаба с другими базисными средствами (сульфасалазин, гидрохлорохин, лефлюномид и парентеральные препараты золота), глюкокортикостероидами, салицилатами, нестероидными противовоспалительными препаратами и анальгетиками.
Комбинированное применение с азатиоприном / 6-меркаптопурином
В клинических исследованиях с участием взрослых с болезнью Крона, увеличение частоты злокачественных новообразований и серьезных побочных реакций, связанных с инфекциями, наблюдалось в группе пациентов, у которых применялось комбинированное применение адалимумаба с азатиоприном / 6-меркаптопурином по сравнению с монотерапией адалимумабом.
Одновременное применение с генно-инженерными биологическими противоревматическими препаратами, в том числе антагонистами ФНО
Тяжелые инфекции наблюдались в клинических исследованиях при одновременном применении анакинры и другого антагониста ФНО, этанерцепта, при этом не наблюдалось улучшения клинического эффекта по сравнению с применением этанерцепта в виде монотерапии. Исходя из природы побочных реакций, наблюдаемых при одновременном применении этанерцепта и анакинры, можно предположить возникновение аналогичных токсических эффектов при одновременном применении анакинры с другими антагонистами ФНО. Таким образом, одновременное применение адалимумаба с анакинрой противопоказано.
Одновременное применение адалимумаба с другими биологическими базовыми противоревматическими средствами (например, анакинрой, абатацептом) или другими антагонистами ФНО сопряжено с повышенным риском возникновения инфекций и других побочных реакций, и поэтому противопоказано.
Особые указания
Инфекции
Применение адалимумаба не следует начинать у пациентов с активными инфекционными заболеваниями, включающими хронические или очаговые инфекции, до купирования инфекции. У пациентов, у которых был контакт с туберкулезом, а также пациентов, посещавших места с высоким уровнем заболеваемости туберкулезом или такими эндемичными микозами, как гистоплазмоз, кокцидиомикоз или бластомикоз, риск и эффективность лечения адалимумабом должны оцениваться до начала терапии (см. Другие оппортунистические инфекции).
Как и в случае с другими антагонистами ФНО, пациенты должны быть тщательно обследованы на наличие инфекционных заболеваний до, во время и после лечения адалимумабом.
Пациенты, у которых развилось инфекционное заболевание во время лечения адалимумабом, должны быть выявлены и полностью обследованы. Применение адалимумаба должно быть приостановлено, если у пациента развивается серьезное инфекционное осложнение или сепсис, при этом соответствующая антибактериальная и противогрибковая терапия должна проводиться до излечения инфекционного заболевания.
С осторожностью следует назначать адалимумаб пациентам с рецидивирующими инфекциями в анамнезе и при наличии условий, предрасполагающих к инфекционным осложнениям.
Туберкулез
Риск развития активного туберкулеза или активации латентного туберкулеза имеется при приеме всех блокаторов ФНО, в том числе адалимумаба. Частота реактивации туберкулеза была особенно выше при дозах адалимумаба, превышавших рекомендованные значения.
До начала терапии адалимумабом все пациенты должны быть обследованы на предмет как активной, так и на неактивной (латентной) туберкулезной инфекции. Эта оценка должна включать подробный анамнез заболевания, с учетом возможных контактов с больными активными формами туберкулеза и предыдущей или текущей иммуносупрессивной терапией, а также необходимые скрининговые обследования (в том числе рентгенография в области грудной клетки, туберкулиновый тест). Лечение скрытой туберкулезной инфекции должно быть проведено до начала терапии адалимумабом. Если диаметр папулы после кожной туберкулиновой пробы на скрытую туберкулезную инфекцию больше 5 мм, то эта проба считается положительной, даже если до этого проводилась вакцинация бациллой Calmette-Guerin (BCG или БЦЖ).
Возможность наличия латентной туберкулезной инфекции должна приниматься во внимание особенно у тех пациентов, которые иммигрировали из страны с высокой заболеваемостью туберкулезом или путешествовали в такую страну, либо у тех, кто был в контакте с больным активной формой туберкулеза.
Если диагностирован активный туберкулез, нельзя начинать терапию адалимумабом.
В том случае, если диагностирован латентный туберкулез, следует проводить превентивную терапию до начала лечения адалимумабом согласно локальным рекомендациям. Превентивная противотуберкулезная терапия до начала лечения адалимумабом также должна назначаться тем пациентам, которые были подвержены факторам риска туберкулеза, даже при отрицательной туберкулиновой пробе. Решение о проведении противотуберкулезной терапии у таких пациентов должно приниматься только с учетом риска латентной туберкулезной инфекции и риска, связанного с противотуберкулезной терапией. Лечение назначается фтизиатром.
Противотуберкулезное лечение пациентов с латентной туберкулезной инфекцией снижает риск реактивации туберкулеза при лечении этих пациентов адалимумабом. Однако риск развития активного туберкулеза или активации латентного туберкулеза существует даже у пациентов, прошедших скрининг и/или противотуберкулезную терапию, поэтому необходимо тщательное наблюдение за пациентами в процессе терапии с целью своевременного выявления симптомов активного туберкулеза, особенно ввиду того, что тесты на скрытую туберкулезную инфекцию часто бывают ложно-негативными. Риск ложно-негативных результатов внутрикожных туберкулиновых проб должен приниматься во внимание особенно у больных в тяжелом состоянии или иммунокомпрометированных больных.
Пациентов следует проинформировать о необходимости обращения к врачу при появлении симптомов (персистирующий кашель, потеря массы тела, субфебрильная лихорадка), указывающих на развитие туберкулезной инфекции.
Другие оппортунистические инфекции
У пациентов, получавших адалимумаб, наблюдались оппортунистические инфекции, включающие грибковые инфекции. Эти инфекции требуют своевременной диагностики и адекватного лечения.
Пациенты, у которых возникает лихорадка, недомогание, потеря массы тела, обильное потоотделение, кашель, одышка и/или инфильтраты в легких на рентгенограмме, либо другие выраженные системные нарушения с развитием шокового состояния либо без него, должны немедленно обратиться к врачу для проведения диагностических мероприятий. У пациентов, которые пребывали в зонах, эндемичных по различным микозам, следует предполагать развитие грибковых инфекций. Такие пациенты находятся в группе риска развития гистоплазмоза или другой грибковой инфекции, и врачи, следовательно, должны начать эмпирическую противогрибковую терапию до идентификации патогена(-ов). Анализы антиген-антитело на гистоплазмоз могут быть отрицательными у некоторых пациентов с активной инфекцией. По возможности, решение о назначении эмпирической противогрибковой терапии у таких пациентов должно приниматься после консультации врачом с квалификацией в диагностике и лечении грибковых инфекций, при этом следует принимать во внимание, как риск тяжелой грибковой инфекции, так и риски, связанные с противогрибковой терапией. Пациентам, у которых развилась тяжелая грибковая инфекция, рекомендуется прекратить прием блокаторов ФНО до момента излечения инфекции.
Реактивация гепатита В
Применение блокаторов ФНО связано с реактивацией вируса гепатита В (ВГВ) у пациентов, которые являются хроническими носителями этого вируса. В некоторых случаях реактивация ВГВ, возникающая в связи с приемом блокаторов ФНО, приводила к летальному исходу. Большая часть этих случаев возникала у пациентов, принимающих другие медикаменты, которые подавляли иммунную систему, что также могло внести свой вклад в реактивацию ВГВ. У пациентов с риском ВГВ инфекции должна проводиться диагностика первичных симптомов ВГВ инфекции до начала терапии блокаторами ФНО. Следует с осторожностью назначать блокаторы ФНО тем пациентам, которые являются носителями ВГВ. Те пациенты, которые являются носителями ВГВ и нуждаются в лечении блокаторами ФНО, должны быть тщательно обследованы для выявления признаков активной ВГВ инфекции во время терапии и через несколько месяцев после окончания терапии. Отсутствуют достоверные данные о безопасности или эффективности лечения носителей ВГВ противовирусными препаратами совместно с блокаторами ФНО для предотвращения реактивации ВГВ. У пациентов, у которых развивается реактивация ВГВ, применение адалимумаба следует приостановить, и должна быть начата эффективная противовирусная терапия с соответствующим поддерживающим лечением.
Неврологические осложнения
Применение антагонистов ФНО, включая адалимумаб, связано с редкими случаями возникновения или осложнения клинических проявлений и/или рентгенологических признаков демиелинизирующих заболеваний центральной нервной системы, включая рассеянный склероз и периферические демиелинизирующие заболевания, включая синдром Гийена-Барре. Следует с осторожностью назначать адалимумаб пациентам с демиелинизирующими заболеваниями центральной и периферической нервной системы (текущими или в анамнезе).
Злокачественные новообразования
Существует более высокий риск развития лимфомы у пациентов с ревматоидным артритом, который характеризуется длительным, тяжелым воспалением, что осложняет оценку степени риска. Во время длительных открытых испытаний адалимумаба средний уровень злокачественных образований был сходен с тем, который ожидался для общей популяции данного возраста, пола и расы. На основании имеющихся данных нельзя исключить возможный риск развития лимфом или других злокачественных новообразований у пациентов, применяющих блокатор ФНО.
Сообщалось о злокачественных новообразованиях, часть которых приводит к летальному исходу у детей и взрослых, получавших лечение блокаторами ФНО. Приблизительно в половине случаев развивались лимфомы, как ходжкинские, так и неходжкинские. В других случаях были представлены различные злокачественные новообразования, включая редкие злокачественные новообразования, связанные с иммуносупрессией. Злокачественные новообразования возникали в среднем через 30 месяцев терапии. Большинство пациентов получали сопутствующее лечение иммунодепрессантами.
Имеются редкие постмаркетинговые сообщения о гепатоспленарной Т-клеточной лимфоме (ГСТКЛ), редкой агрессивной лимфоме, которая возникала у пациентов, получающих адалимумаб, и нередко приводила к летальному исходу. Большинство пациентов изначально получали терапию инфликсимабом, а также сопутствующую терапию воспалительных заболеваний толстого кишечника азатиоприном или 6-меркаптопурином. Причинно-следственная связь ГСТКЛ с приемом адалимумаба не доказана.
Не проводилось исследований, включающих пациентов с анамнезом злокачественных новообразований, либо в ходе которых лечение адалимумабом продолжалось у пациентов с развившимся злокачественным новообразованием. Таким образом, следует проявлять дополнительную осторожность при применении адалимумаба у таких пациентов.
Все пациенты, и в особенности пациенты, ранее получавшие продолжительную терапию иммунодепрессантами или ПУВА-терапию псориаза, должны обследоваться на наличие, не связанного с меланомой, рака кожи, который развился до или во время лечения адалимумабом.
Случаи острого или хронического лейкоза описывались в связи с постмаркетинговым использованием блокаторов ФНО для лечения ревматоидного артрита и по другим показаниям. У пациентов с ревматоидным артритом выше риск развития лейкемии (до двукратного), чем в общей популяции, даже в отсутствие терапии блокаторами ФНО.
Аллергия
Серьезные аллергические реакции, связанные с приемом адалимумаба, были редки во время клинических испытаний. В постмаркетинговых наблюдениях серьезные аллергические реакции, включающие анафилактический шок, после приема адалимумаба описывались очень редко. Если возникает анафилактическая реакция или другие серьезные аллергические реакции, следует немедленно прекратить применение адалимумаба и назначить соответствующую противоаллергическую терапию.
Гематологические осложнения
Имелись редкие сообщения о развитии панцитопении, включая апластическую анемию при применении блокаторов ФНО. Изредка сообщалось о побочных реакциях со стороны системы крови, включающих значительную цитопению (в том числе тромбоцитопению, лейкопению) при лечении адалимумабом. Причинная связь этих сообщений с приемом адалимумаба остается неясной. Всем пациентам следует рекомендовать незамедлительно обращаться к врачу, если у них развиваются симптомы, указывающие на нарушения системы крови (в т. ч. персистирующая лихорадка, гематомы, кровотечение, бледность) при лечении адалимумабом. При подтвержденных значительных гематологических нарушениях лечение адалимумабом следует приостановить.
Вакцинация
Пациентам детского возраста рекомендуется по возможности пройти полную вакцинацию в соответствии с текущим графиком иммунизации до начала терапии адалимумабом.
Пациенты, принимающие адалимумаб, могут получать попутно вакцинацию, за исключением живых вакцин.
Хроническая сердечная недостаточность (ХСН)
Не проводилось исследований применения адалимумаба у пациентов с хронической сердечной недостаточностью (ХСН), однако при проведении клинических испытаниях другого антагониста ФНО, наблюдался более высокий уровень связанных с ХСН нежелательных явлений, включая развитие ХСН и прогрессирование ХСН. Случаи прогрессирования ХСН также описывались у пациентов, принимающих адалимумаб. Следует с осторожностью назначать адалимумаб пациентам с сердечной недостаточностью, и проводить тщательное наблюдение таким пациентам.
Аутоиммунные процессы
Лечение адалимумабом может приводить к формированию аутоиммунных антител.
Влияние длительного лечения на развитие аутоиммунных заболеваний не изучено.
Если у пациента развиваются симптомы, предполагающие волчаночноподобный синдром в результате лечения адалимумабом, следует прекратить использование препарата.
Пожилые пациенты
Частота возникновения серьезных инфекций среди пациентов старше 65 лет, принимавших адалимумаб, была выше, чем у пациентов моложе 65 лет. 9,5% от общего числа пациентов, принимавших адалимумаб было старше 65 лет и приблизительно 2,0% было старше 75 лет.
Адалимумаб следует назначать с осторожностью у пожилых пациентов в связи с высокой вероятностью возникновения инфекционных заболеваний. Различий в эффективности у данной группы пациентов по сравнению с более молодыми пациентами не выявлено, корректировка дозы не требуется.
Дети
Эффективность и безопасность применения адалимумаба у детей показана только для лечения идиопатического ювенильного артрита от 2 лет и болезни Крона (среднетяжелой или тяжелой степени) у пациентов от 6 лет и старше.
Возможность хранения препарата Хумира® в шприцах при комнатной температуре
При необходимости (например, во время путешествия), препарат Хумира® допускается хранить при комнатной температуре (до 25°C) в защищенном от света месте не более 14 ней. С момента извлечения из холодильника, шприц должен быть использован в течение 14 дней, если шприц после извлечения из холодильника не будет использован в течение этого срока, он должен быть уничтожен. Для удобства рекомендуется записать дату извлечения шприца из холодильника и срок, в течение которого следует использовать препарат.
Влияние на способность к управлению автомобилем и другими механизмами
Препарат Хумира® может оказывать незначительное влияние на способность управлять транспортными средствами и другими механизмами, так как на фоне применения препарата могут наблюдаться головокружение и нарушение зрения (см. раздел «Побочное действие»).
Форма выпуска
Раствор для подкожного введения 40 мг/0,8 мл.
Препарат в однодозовом шприце
По 0,8 мл в однодозовые шприцы из бесцветного стекла. По 1 шприцу вместе с 1 салфеткой, пропитанной 70% изопропиловым спиртом, в ламинированной полиэтиленом бумаге, в блистере из ПВХ и ламинированной бумаги. По 1 или 2 блистера вместе с инструкцией по применению в пачке картонной.
Препарат во флаконе
По 0,8 мл во флаконы из бесцветного стекла, укупоренные резиновой пробкой и алюминиевым колпачком с полипропиленовой крышкой.
Набор для однодозового введения содержит компоненты, необходимые для одной подкожной инъекции:
1. один флакон из бесцветного стекла, содержащий 0,8 мл препарата;
2. один пластиковый шприц с соединением Люэра в блистере;
3. одну насадку на флакон в блистере;
4. одну инъекционную иглу с соединением Люэра, с полипропиленовым защитным колпачком и полипропиленовым защитным чехлом в блистере;
5. две салфетки, пропитанные 70 % изопропиловым спиртом, в ламинированной полиэтиленом бумаге.
Один набор вместе с инструкцией по применению в пачке картонной.
По две пачки картонные, каждая содержащая 1 набор для однодозового введения и инструкцию по применению, в пачке картонной.
Условия хранения
При температуре от 2°С до 8°С в защищенном от света месте. Не замораживать. Хранить в недоступном для детей месте.
Срок годности
2 года. Не применять по истечении срока годности, указанного на упаковке.
Условия отпуска
По рецепту.
Владелец регистрационного удостоверения
ООО «ЭббВи», Россия
125171, г. Москва, Ленинградское шоссе, д. 16 А, стр. 1
Производитель
Vetter Farma-Fertigung GmbH & Со.KG, Schutzenstrasse 87, Ravensburg, 88212, Germany.
Веттер Фарма-Фертигунг ГмбХ и Ко.КГ, Шютценштрассе 87, Равенсбург, 88212, Германия.
Vetter Farma-Fertigung GmbH & Со. KG, Eisenbahn strasse 2-4, 88085 Langenargen, Germany.
Веттер Фарма-Фертигунг ГмбХ и Ко. КГ, Айзенбан штрассе 2-4, 88085 Лангенарген, Германия.
Упаковано
Vetter Farma-Fertigung GmbH & Со.KG, Schutzenstrasse 87, Ravensburg, 88212, Germany.
Веттер Фарма-Фертигунг ГмбХ и Ко.КГ, Шютценштрассе 87, Равенсбург, 88212, Германия.
или
Vetter Farma-Fertigung GmbH & Со. KG, Eisenbahn strasse 2-4, 88085 Langenargen, Germany.
Веттер Фарма-Фертигунг ГмбХ и Ко.КГ, Айзенбан штрассе 2-4, 88085 Лангенарген, Германия.
или
ЗАО «ОРТАТ», Россия
157092, Костромская обл., Сусанинский р-н, с. Северное, мкр-н Харитоново, тел./факс (4942) 650-806
Представительство в России:
ООО «ЭббВи»
141400 Московская область, г. Химки, ул. Ленинградская, владение 39, стр. 5, Химки Бизнес Парк.
тел. (495) 258 42 70
факс (495) 258 42 71
ИНСТРУКЦИЯ ПО ПОДГОТОВКЕ И ПРОВЕДЕНИЮ ИНЪЕКЦИИ ПРЕПАРАТА ХУМИРА® В ОДНОДОЗОВОМ ШПРИЦЕ
1) Подготовка
• Тщательно вымойте руки.
• Достаньте из упаковки и положите на чистую поверхность один шприц с препаратом Хумира® и одну пропитанную спиртом салфетку.
• Убедитесь, что срок хранения препарата Хумира®, указанный на шприце, не истек.
• Препарат Хумира® представляет собой прозрачную, бесцветную жидкость. Не используйте препарат, если жидкость мутная, содержит хлопья или частицы или изменила свой цвет.
2) Выбор и подготовка места для инъекции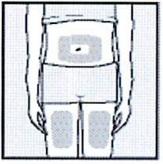
• Выберите место на животе или передней поверхности бедра.
• Места инъекций и стороны следует менять.
• Каждое следующее место введения должно отступать от предыдущего как минимум на 3 см.
• Нельзя вводить препарат в место на коже, где имеется болезненность, покраснение, уплотнение или кровоподтек. Эти признаки могут указывать на наличие инфекции.
• Место укола необходимо обработать спиртовой салфеткой круговыми движениями.
3) Введение препарата Хумира® 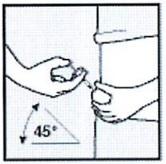
• Не встряхивайте шприц.
• Снимите колпачок с иглы, не дотрагиваясь до иглы и избегая прикосновения к другим поверхностям.
• Одной рукой возьмите в складку обработанную кожу.
• В другую руку возьмите шприц, держа его под углом 45° к поверхности кожи, градуированной поверхностью вверх.
• Одним быстрым движением полностью введите иглу в кожную складку.
• После введения иглы отпустите складку кожи.
• Введите весь раствор в течение 2-5 секунд.
• После введения раствора (когда шприц будет пустым) извлеките иглу из кожи, под тем же углом.
• Кусочком марли слегка прижмите область инъекции в течение 10 секунд, но ни в коем случае не трите поверхность. Из места инъекции может выделиться небольшое количество крови. При желании можно воспользоваться пластырем.
• После инъекции шприц повторно не использовать.
ИНСТРУКЦИЯ ПО ПОДГОТОВКЕ И ПРОВЕДЕНИЮ ИНЪЕКЦИИ ПРЕПАРАТА ХУМИРА® ВО ФЛАКОНЕ
1) Подготовка
• Убедитесь в том, что Вы знаете какое количество (объем) препарата нужно ввести.
• Тщательно вымойте руки.
• Возьмите из картонной упаковки одну коробку, содержащую один шприц, одну насадку на флакон, один флакон, две спиртовые салфетки и одну иглу. Если в картонной упаковке осталась еще одна коробка с набором для следующей инъекции, немедленно уберите ее в холодильник.
• Проверьте срок годности препарата, указанный на коробке. НЕ ИСПОЛЬЗУЙТЕ набор после окончания его срока годности.
• Положите следующие предметы на чистую поверхность, на данном этапе НЕ вытаскивайте их из индивидуальной упаковки.
Один шприц объемом 1 мл (1)
Одну насадку на флакон (2)
Один флакон препарата Хумира®, раствор для инъекций (3)
Две спиртовые салфетки (4)
Одну иглу (5)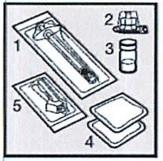
• Препарат Хумира® представляет собой прозрачную, бесцветную жидкость. Не используйте препарат, если жидкость мутная, содержит хлопья или частицы или изменила свой цвет.
2) Подготовка дозы препарата Хумира® к введению
Общее правило: ничего НЕ выбрасывайте до окончания инъекции препарата.
• Подготовьте иглу, частично сняв с нее упаковку, открытую со стороны, ближайшей к желтому соединительному колпачку иглы. Снимите упаковку ровно настолько, чтобы открыть желтый соединительный колпачок. Держите упаковку открытым концом вверх.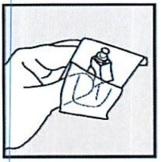
• Снимите белый пластиковый колпачок с флакона так, чтобы увидеть верхнюю часть пробки флакона.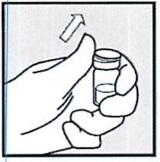
• Одной из спиртовых салфеток протрите пробку флакона. После этого НЕ прикасайтесь к пробке флакона.
• Откройте упаковку насадки на флакон, но не вытаскивайте ее из упаковки.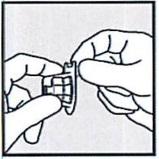
• Флакон держите пробкой вверх.
• Не вынимая насадку на флакон из упаковки, соедините ее с пробкой флакона, надавливая насадкой на пробку до тех пор, пока она не встанет с щелчком на место.
• Когда Вы убедитесь в том, что насадка соединена с флаконом, снимите с нее упаковку.
• Осторожно поставьте флакон с насадкой на чистую рабочую поверхность. Будьте аккуратны, флакон не должен упасть. НЕ ПРИКАСАЙТЕСЬ к насадке.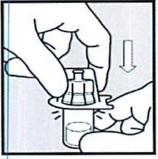
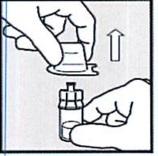
• Подготовьте шприц, частично сняв с него упаковку, открытую со стороны, ближайшей к белому шток-поршню.
• Снимите упаковку ровно настолько, чтобы открыть белый шток-поршень, но не вытаскивайте шприц из упаковки.
• Держите упаковку шприца и МЕДЛЕННО вытяните белый шток-поршень, так чтобы объем превышал необходимую дозу на 0,1 мл. (Например, если назначенная доза составляет 0,5 мл, вытяните белый шток-поршень на 0,6 мл). НИКОГДА не вытягивайте поршень дальше положения, соответствующего 0,9 мл, вне зависимости от назначенной дозы.
• Вы скорректируете объем в соответствии с назначенной дозой позднее.
• НЕ ВЫТЯГИВАЙТЕ белый шток-поршень из шприца полностью.
• ПРИМЕЧАНИЕ:
Если белый шток-поршень полностью вынут из шприца, шприц использовать нельзя. НЕ ПЫТАЙТЕСЬ вставить белый шток-поршень обратно.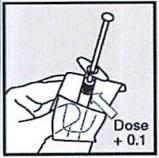
• НЕ ИСПОЛЬЗУЙТЕ белый шток-поршень, чтобы вынуть шприц из упаковки. Вытащите шприц из упаковки, при этом шток-поршень должен остаться в установленном положении. Никогда НЕ ОПУСКАЙТЕ шприц.
• Крепко держите насадку на флакон. Введите наконечник шприца в насадку и поверните одной рукой шприц по часовой стрелке до упора. Не прилагайте излишние усилия при повороте шприца по часовой стрелке до упора.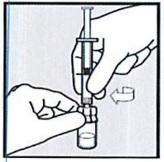
• Держа флакон, нажмите на шток-поршень и полностью опустите его. Этот шаг важен для получения правильной дозы препарата. Удерживайте белый шток-поршень внутри и переверните шприц с флаконом.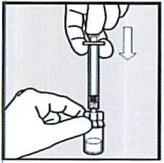
• МЕДЛЕННО потяните на себя белый шток-поршень до отметки, на 0,1 мл превышающей требуемую дозу. Это важно для получения правильной дозы. Вы скорректируете дозу на этапе 4 (Подготовка дозы препарата). Если назначенная доза составляет 0,5 мл, вытяните белый шток-поршень на 0,6 мл. Вы увидите, как жидкость из флакона заполняет шприц.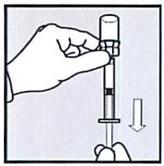
• Надавите на белый шток-поршень, так чтобы вернуть жидкость во флакон. Снова МЕДЛЕННО потяните на себя белый шток-поршень до отметки, на 0,1 мл превосходящей требуемую дозу, это важно для получения правильной дозы и предотвращения образования пузырьков воздуха и воздушных зазоров. Вы скорректируете дозу на этапе 4 (Подготовка дозы препарата).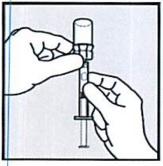
• Если Вы видите, что в шприце остались пузырьки воздуха или воздушные зазоры, Вы можете повторить описанную процедуру до трех раз. НЕ ТРЯСИТЕ шприц.
ПРИМЕЧАНИЕ:
• Если белый шток-поршень полностью вынут из шприца, шприц использовать нельзя. НЕ ПЫТАЙТЕСЬ вставить белый шток-поршень обратно.
• Все еще держа шприц вертикально, отсоедините от шприца насадку на флакон вместе с флаконом, повернув адаптер флакона другой рукой. Убедитесь в том, что вместе с флаконом Вы отсоединили от шприца и насадку. НЕ ПРИКАСАЙТЕСЬ к кончику шприца.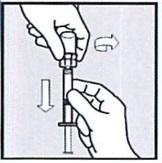
• Если вблизи кончика шприца заметны крупные пузырьки воздуха или воздушные зазоры, МЕДЛЕННО надавите на белый шток-поршень до тех пор, пока жидкость не начнет заполнять кончик шприца. НЕ НАЖИМАЙТЕ на белый шток-поршень после достижения отметки необходимой дозы.
• Например, если назначенная доза составляет 0,5 мл, НЕ НАЖИМАЙТЕ на белый шток-поршень после достижения отметки 0,5 мл. Убедитесь в том, что объем жидкости, оставшейся в шприце, по крайней мере, не меньше назначенной дозы. Если оставшийся объем меньше назначенной дозы, не используйте этот шприц.
• Свободной рукой возьмите упаковку с иглой таким образом, чтобы желтый соединительный колпачок был направлен вниз.
• Держа шприц направленным вверх, введите кончик шприца в желтый соединительный колпачок иглы и поверните шприц до упора, как показано стрелкой на картинке, приведенной ниже. Теперь игла соединена с шприцом.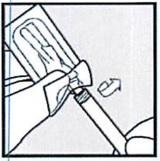
• Снимите упаковку с иглы, но НЕ УДАЛЯЙТЕ защитный колпачок иглы.
• Положите шприц на чистую рабочую поверхность. Незамедлительно переходите к выбору области для инъекции и подготовке дозы.
3) Выбор и подготовка области для инъекции
• Выберите область на бедре или животе.
• Новое место инъекции должно находиться на расстоянии, по крайней мере, 3 см от предыдущего места введения препарата.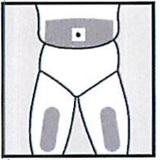
• Нельзя вводить препарат в место на коже, где имеется болезненность, покраснение, уплотнение или кровоподтек. Эти признаки могут указывать на наличие инфекции.
• Для снижения риска инфицирования обработайте область инъекции второй спиртовой салфеткой. Не ПРИКАСАЙТЕСЬ к области введения препарата до инъекции.
4) Подготовка дозы
• Возьмите шприц таким образом, чтобы игла была направлена вверх.
• Другой рукой перекиньте розовый колпачок иглы к шприцу.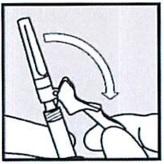
• Снимите защитный колпачок, потянув его вверх другой рукой.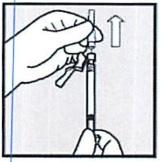
• НЕ ПРИКАСАЙТЕСЬ к игле.
• НЕ КЛАДИТЕ шприц после того, как сняли с иглы колпачок.
• НЕ ПЫТАЙТЕСЬ надеть на иглу снятый защитный колпачок.
• Держите шприц на уровне глаз, при этом игла должна быть направлена вверх. Вы должны четко видеть количество препарата в шприце. Будьте осторожны, чтобы препарат не попал Вам в глаза.
• Еще раз проверьте, какое количество препарата Вам нужно отмерить.
• Аккуратно надавите на белый шток-поршень таким образом, чтобы в шприце осталось назначенное количество препарата. Избыток препарата может выйти из иглы. НЕ ПРОМОКАЙТЕ иглу или шприц.
5) Введение препарата Хумира®
• Свободной рукой осторожно соберите складку кожи обработанной области и крепко держите ее.
• Другой рукой возьмите шприц и держите его под углом 45° к коже.
• Одним быстрым, коротким движением полностью введите иглу в кожу.
• Отпустите кожную складку.
• Надавите на белый шток-поршень, чтобы ввести препарат. Введите все лекарство полностью.
• Когда шприц окажется пустым, удалите иглу из кожи. Будьте осторожны, извлеките иглу под тем же углом, под каким ее вводили.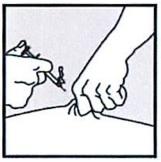
• Аккуратно накиньте розовый колпачок на иглу до щелчка. Положите шприц с иглой на рабочую поверхность.
• НЕ НАДЕВАЙТЕ снятый защитный колпачок на иглу.
• После инъекции шприц, флакон, иглу, колпачок иглы и насадку на флакон повторно НЕ ИСПОЛЬЗОВАТЬ.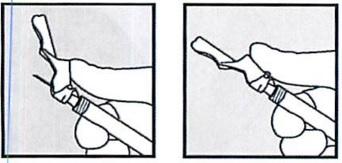
• Кусочком марли надавите на область введения препарата в течение 10 секунд.
• Может быть небольшое кровотечение. НЕ ТРИТЕ место инъекции. Область инъекции можно заклеить пластырем.


Добавить отзыв или комментарий